薬剤師国家試験 令和07年度 第110回 - 一般 実践問題 - 問 324,325
ある薬局で、服薬指導の内容と服薬アドヒアランスとの関係を明らかにするために、この薬局で過去5年間に降圧薬を調剤された成人患者を対象として、薬歴を用いて後ろ向きに調査を行い、学会発表することを計画している。研究に用いるデータは、患者名はわからないように集計、解析する予定である。
調査対象となる患者全員に個別に説明し同意を取得するのは困難なので、研究概要の薬局内へのポスター掲示と薬局ホームページへの掲載によりいつでも質問を受け付けることができるようにすることで、倫理審査委員会の承認を受ける予定である。なお、この研究にかかる費用はこの薬局で負担することにした。
問324(実務)
この薬局で研究のために作成するポスターに記載する内容として必要なのはどれか。2つ選べ。
1 研究目的
2 研究協力の拒否の方法
3 研究に携わっている全員の連絡先
4 倫理審査委員会の委員の氏名
5 この研究に要する費用
問325(法規・制度・倫理)
当該研究に関して倫理審査委員会に提出する申請書類を作成する際に、遵守することが求められるのはどれか。1つ選べ。
1 医薬品の臨床試験の実施の基準に関する省令
2 人を対象とする生命科学・医学系研究に関する倫理指針
3 医薬品の安全性に関する非臨床試験の実施の基準に関する省令
4 日本薬局方
5 臨床研究法
 REC講師による詳細解説! 解説を表示
REC講師による詳細解説! 解説を表示
-
問324 解答 1、2
薬局において、過去5年間の薬歴を用い、服薬指導の内容と服薬アドヒアランスとの関係を調べる研究を行う場合、既存試料・情報を用いた観察研究に該当し、人を対象とする生命科学・医学系研究に関する倫理指針を遵守する必要がある。
この指針において、インフォームド・コンセントを受ける手続きについて、以下のように規定されている。

本研究は、薬局が保有している既存の情報を利用し、試料を用いない研究であり、インフォームド・コンセントの取得は義務ではない。
本研究では、インフォームド・コンセントを取得しない場合、以下の対応が必要である。
・当該研究の実施について、①〜⑦の事項を研究対象者等に通知し、又は研究対象者等が容易に知り得る状態に置いていること
① 情報の利用目的及び利用方法(選択肢1)
② 利用する情報の項目
③ 利用を開始する予定日
④ 利用する者の範囲
⑤ 情報の管理について責任を有する者の氏名又は名称
⑥ 研究対象者等の求めに応じて、研究対象者が識別される情報の利用を停止する旨
⑦ ⑥の研究対象者等の求めを受け付ける方法
・当該研究が実施又は継続されることについて、原則として、研究対象者等が拒否できる機会を保障すること(選択肢2)
問325 解答 2
医学研究の目的や方法により、遵守すべき指針や法令は下記のとおり大別される。
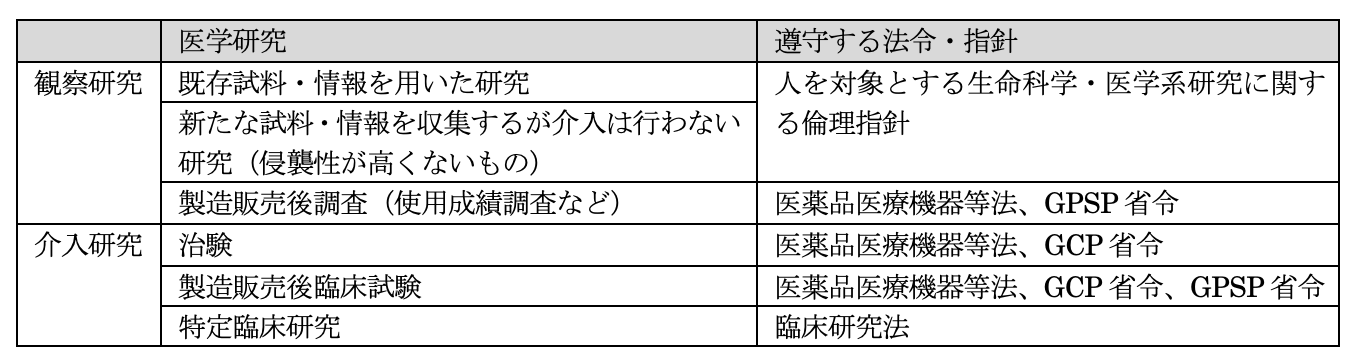
1 誤
医薬品の臨床試験の実施の基準に関する省令(GCP省令)は、被験者の人権の保護、安全の保持及び福祉の向上を図り、治験の科学的な質及び成績の信頼性を確保するため、医薬品の臨床試験の実施に係る基準を定めたものである。
2 正
本研究は、既存試料・情報を用いた観察研究に該当し、人を対象とする生命科学・医学系研究に関する倫理指針を遵守することが求められる。
3 誤
医薬品の安全性に関する非臨床試験の実施の基準に関する省令(GLP省令)は、製造販売業者等が行う医薬品の非臨床安全性試験に関する遵守事項を定め、その適正な実施を確保し、もって医薬品の安全性に関する非臨床試験に関する資料の信頼性の確保を図ることを目的としたものである。
4 誤
日本薬局方は、医薬品医療機器等法により、医薬品の性状及び品質の適正を図るため、厚生労働大臣が薬事審議会の意見を聴いて定めた医薬品の規格基準書である。
5 誤
臨床研究法の遵守が義務づけられているのは、以下に該当する研究である。
・未承認・適応外の医薬品等の臨床研究
・製薬企業等から研究資金等の提供を受けて実施する医薬品等の臨床研究
- この過去問解説ページの評価をお願いします!
-
評価を投稿
 REC講師による詳細解説! 解説を表示
REC講師による詳細解説! 解説を表示


