薬剤師国家試験 令和05年度 第108回 - 必須問題 - 問 10
マグネシウムに関する記述のうち、誤っているのはどれか。1つ選べ。
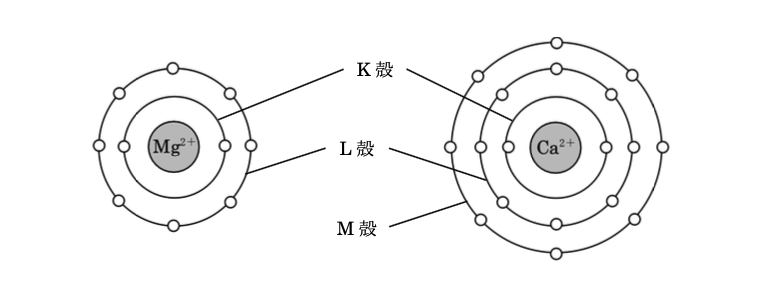
1 マグネシウムイオンは、カルシウムイオンに比べてイオン半径が小さい。
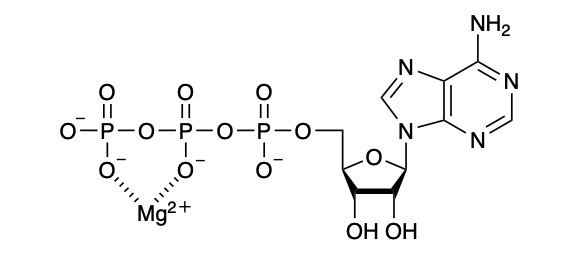
2 マグネシウムイオンは、ルイス酸としてATPのリン酸基と結合する。
3 空気中で金属マグネシウムが燃焼すると、酸化マグネシウムとなる。
4 マグネシウムは、典型元素である。
5 酸化マグネシウムは、酸性酸化物である。
 REC講師による詳細解説! 解説を表示
REC講師による詳細解説! 解説を表示
-
 解説動画1 ( 06:05 )
解説動画1 ( 06:05 )
- ※ この解説動画は 60 秒まで再生可能です
|
ビデオコントロール | |
|
|
| 再生速度 |
- この過去問解説ページの評価をお願いします!
-
- わかりにくい
- とてもわかりやすかった