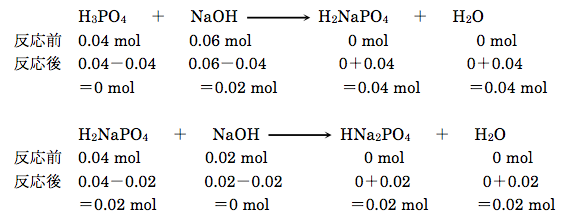薬剤師国家試験 平成25年度 第98回 - 一般 理論問題 - 問 95
0.10 mol/Lリン酸400 mLと0.20 mol/L水酸化ナトリウム300 mLを混合した水溶液の25℃におけるpHに最も近いのはどれか。1つ選べ。
ただし、リン酸のpKa1=2.12、pKa2=7.21、pKa3=12.32(各25℃)とする。また、log2=0.30、log3=0.48とする。
1 4.7
2 6.9
3 7.2
4 7.7
5 9.8
 REC講師による詳細解説! 解説を表示
REC講師による詳細解説! 解説を表示
-
解答 3
0.10 mol/Lリン酸400 mL(リン酸を0.04 mol含有)と0.20 mol/L水酸化ナトリウム300 mL(水酸化ナトリウムを0.06 mol含有)と混合した水溶液中では、以下のように2段階で反応が進行する。
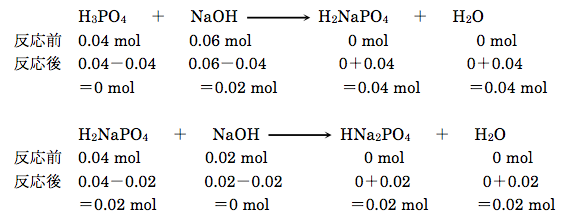
反応した結果、0.02 molのH2NaPO4と0.02 molのH2NaPO4を含む700 mLの溶液が生成する。溶液中には弱酸(H2NaPO4)とその塩(HNa2PO4)が1:1で含まれているため、その溶液のpHはリン酸における2段階目の酸解離指数(pKa2=7.21)とほぼ等しくなる。
したがって、0.10 mol/Lリン酸400 mLと0.20 mol/L水酸化ナトリウム300 mLを混合した水溶液の25℃におけるpHは約7.2となる。
- この過去問解説ページの評価をお願いします!
-
評価を投稿
 REC講師による詳細解説! 解説を表示
REC講師による詳細解説! 解説を表示