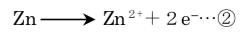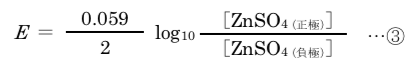薬剤師国家試験 令和02年度 第105回 - 一般 理論問題 - 問 100
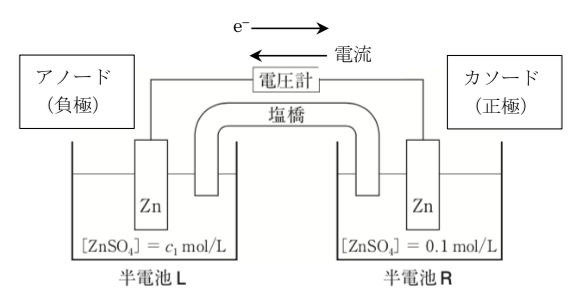
生体における膜電位の原理を理解するためには、濃淡電池の作動原理を知ることが必要である。電解質として用いる硫酸亜鉛の濃度のみが異なる2つの亜鉛半電池を塩橋でつないだ化学電池の模式図を以下に示す。標準圧力下、298Kにおいて半電池Rの硫酸亜鉛の初濃度を0.1 mol/L、半電池Lの硫酸亜鉛の初濃度をc1 mol/Lとする。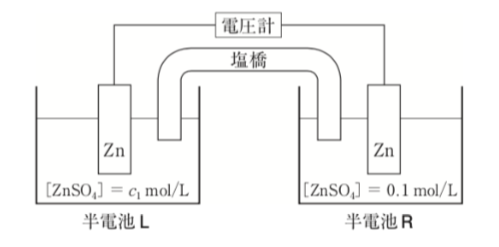
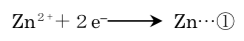
なお、亜鉛半電池の反応は次式で表される。(E °は標準電位を表す)。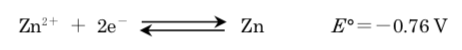
また、硫酸亜鉛は水中では完全に電離し、その活量は濃度に等しいとする。この場合の亜鉛半電池の電極電位E (単位V)は温度298 Kでは次式で表される。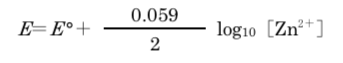
この化学電池に関する記述のうち、正しいのはどれか。2つ選べ。
1 この電池はダニエル電池である。
2 c1=0.01のとき、半電池Lがアノード(負極)となる。
3 この電池の標準起電力は0 Vである。
4 半電池Lと半電池Rの硫酸亜鉛濃度が等しくなった状態の起電力は-0.76 Vである。
5 c1=0.01のとき、この電池の起電力は約+0.059 Vである。
 REC講師による詳細解説! 解説を表示
REC講師による詳細解説! 解説を表示
-
 解説動画1 ( 23:23 )
解説動画1 ( 23:23 )
- ※ この解説動画は 60 秒まで再生可能です
|
ビデオコントロール | |
|
|
| 再生速度 |
- この過去問解説ページの評価をお願いします!
-
- わかりにくい
- とてもわかりやすかった